تعمل "أنظمة كريسبر-كاس" في البكتيريا والفيروسات على تحديد وتدمير التسلسلات الفيروسية الغازية. وهو عبارة عن جهاز مناعي بكتيري وأثري للحماية من الالتهابات الفيروسية. في عام 2012، تم الاعتراف بنظام CRISPR-Cas كنظام الجينوم أداة التحرير. منذ ذلك الحين، تم تطوير مجموعة واسعة من أنظمة كريسبر-كاس ووجدت تطبيقات في مجالات مثل العلاج الجيني والتشخيص والبحوث وتحسين المحاصيل. ومع ذلك، فإن أنظمة CRISPR-Cas المتاحة حاليًا لها استخدام سريري محدود بسبب تكرار حدوث التحرير خارج الهدف، وطفرات الحمض النووي غير المتوقعة والمشاكل الوراثية. أعلن الباحثون مؤخرًا عن نظام CRISPR-Cas جديد يمكنه استهداف وتدمير mRNA و البروتينات المرتبطة بالأمراض الوراثية المختلفة بشكل أكثر دقة دون تأثير خارج الهدف ومشاكل وراثية. يُسمى Craspase، وهو أول نظام CRISPR-Cas يظهر بروتين وظيفة التحرير. وهو أيضًا أول نظام يمكنه تحرير كل من RNA و بروتين. ولأن Craspase يتغلب على العديد من القيود التي تعيب أنظمة CRISPR-Cas الحالية، فإنه لديه القدرة على إحداث ثورة في العلاج الجيني، والتشخيص والرصد، والبحوث الطبية الحيوية، وتحسين المحاصيل.
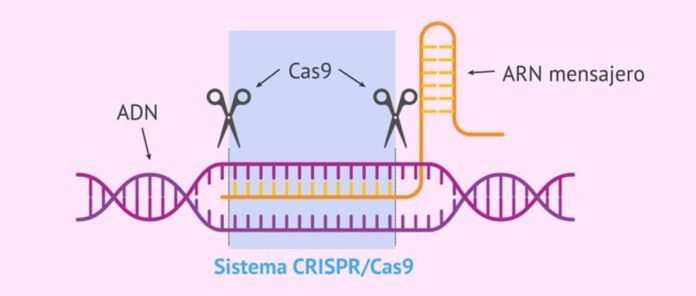
"نظام كريسبر-كاس" هو نظام مناعي طبيعي للبكتيريا والعتائق ضد الالتهابات الفيروسية الذي يحدد ويربط ويتحلل التسلسلات في الجين الفيروسي لحمايته. وهو يتألف من جزأين - الحمض النووي الريبي البكتيري المنقول من الجين الفيروسي المدمج في الجينوم البكتيري بعد الإصابة الأولى (يُسمى كريسبر، وهذا يحدد التسلسل المستهدف للجينات الفيروسية الغازية) ومدمر مرتبط به بروتين يسمى "كريسبر المرتبطة بروتين (Cas)" الذي يربط ويتحلل التسلسلات المحددة في الجين الفيروسي لحماية البكتيريا من الفيروسات.
كريسبر يرمز إلى "التكرارات المتناوبة القصيرة المتجمعة بانتظام والمتباعدة". وهو عبارة عن RNA بكتيري منسوخ يتميز بتكرارات متناوبة.
تم اكتشاف التكرارات المتناغمة (CRISPRs) لأول مرة في متواليات E. كولاي في عام 1987. وفي عام 1995، لاحظ فرانسيسكو موخيكا هياكل مماثلة في العتائق، وكان هو أول من فكر في هذه العناصر كجزء من الجهاز المناعي للبكتيريا والعتائق. في عام 2008، تم إثبات تجريبيًا لأول مرة أن هدف الجهاز المناعي للبكتيريا والعتائق كان DNA أجنبيًا وليس mRNA. اقترحت آلية تحديد التسلسلات الفيروسية وتحللها أنه يمكن استخدام هذه الأنظمة كأداة لتحديد التسلسل الفيروسي تحرير الجينوم. منذ الاعتراف به كأداة لتحرير الجينوم في عام 2012، قطع نظام كريسبر-كاس شوطا طويلا كمعيار راسخ تحرير الجين النظام ووجد مجموعة واسعة من التطبيقات في الطب الحيوي والزراعة والصناعات الدوائية بما في ذلك العلاج الجيني السريري1,2.
مجال واسع من كريسبر-تم بالفعل تحديد أنظمة Cas وهي متاحة حاليًا لرصد وتحرير تسلسل الحمض النووي/الحمض النووي الريبي (DNA) للبحث وفحص الأدوية والتشخيص والعلاج. تنقسم أنظمة كريسبر/كاس الحالية إلى فئتين (الفئة 2 و1) وستة أنواع (النوع الأول إلى الحادي عشر). تحتوي أنظمة الفئة 2 على Cas متعددة البروتينات والتي تحتاج إلى تشكيل مجمع وظيفي لربط أهدافها والعمل على تحقيقها. من ناحية أخرى، تحتوي أنظمة الفئة 2 على Cas واحد كبير فقط بروتين لربط وتحطيم التسلسل المستهدف مما يجعل أنظمة الفئة 2 أسهل في الاستخدام. أنظمة الفئة 2 شائعة الاستخدام هي Cas 9 Type II وCas13 Type VI وCas12 Type V. وقد يكون لهذه الأنظمة تأثيرات جانبية غير مرغوب فيها، مثل التأثير خارج الهدف والسمية الخلوية3,5.
العلاجات الجينية استنادًا إلى أنظمة CRISPR- Cas الحالية لها استخدام سريري محدود بسبب التكرار المتكرر للتحرير خارج الهدف ، وطفرات الحمض النووي غير المتوقعة ، بما في ذلك عمليات حذف أجزاء كبيرة من الحمض النووي والمتغيرات الهيكلية الكبيرة للحمض النووي في كل من المواقع المستهدفة وغير المستهدفة التي تؤدي إلى موت الخلايا ومشاكل وراثية أخرى.
Craspase (أو caspase الموجهة بواسطة CRISPR)
أبلغ الباحثون مؤخرًا عن نظام CRISPER-Cas جديد وهو نظام من الفئة 2 من النوع III-E Cas7-11 مرتبط بهيكل يشبه الكاسبيز. بروتين ومن هنا سمي كاسباس Craspase أو CRISPR الموجهة 5 (الكاسبيز عبارة عن بروتياز السيستين الذي يلعب دورًا رئيسيًا في موت الخلايا المبرمج في تحطيم الهياكل الخلوية). وله تطبيقات محتملة في مجالات مثل العلاج الجيني والتشخيص. Craspase موجه بواسطة RNA ويستهدف RNA ولا يتدخل في تسلسل الحمض النووي. يمكنه استهداف وتدمير mRNA و البروتينات المرتبطة بالأمراض الوراثية المختلفة بشكل أكثر دقة دون التأثير خارج الهدف. وبالتالي، فإن التخلص من الجينات المرتبطة بالأمراض أمر ممكن عن طريق الانقسام عند مستوى الرنا المرسال أو مستوى البروتين. أيضًا، عند ربطه مع إنزيم معين، يمكن أيضًا استخدام Craspase لتعديل وظائف البروتينات. عندما تتم إزالة وظائف RNase والبروتياز، يصبح Craspase معطلاً (dCraspase). ليس لديها وظيفة قطع ولكنها ترتبط بتسلسلات الحمض النووي الريبي (RNA) والبروتين. ولذلك، يمكن استخدام dCraspase في التشخيص والتصوير لرصد وتشخيص الأمراض أو الفيروسات.
Craspase هو أول نظام CRISPR-Cas يُظهر وظيفة تحرير البروتين. وهو أيضًا أول نظام يمكنه تحرير كل من الحمض النووي الريبي (RNA) والبروتين. إنه تحرير الجين تأتي الوظيفة بأقل قدر من التأثيرات غير المستهدفة ولا توجد مشاكل قابلة للتوريث. وبالتالي، من المرجح أن يكون Craspase أكثر أمانًا في الاستخدام السريري والعلاجي من أنظمة CRISPR-Cas الأخرى المتوفرة حاليًا 4,5.
نظرًا لأن Craspase يتغلب على العديد من القيود المفروضة على أنظمة CRISPR-Cas الحالية ، فإن لديه القدرة على إحداث ثورة في العلاج الجيني ، والتشخيصات والمراقبة ، والبحوث الطبية الحيوية ، وتحسين المحاصيل. هناك حاجة إلى مزيد من البحث لتطوير نظام توصيل موثوق به لاستهداف الجينات المسببة للأمراض في الخلايا بدقة قبل إثبات السلامة والفعالية في التجارب السريرية.
***
المراجع:
- Gostimskaya، I. CRISPR-Cas9: تاريخ من اكتشافه والاعتبارات الأخلاقية لاستخدامه في تحرير الجينوم. الكيمياء الحيوية موسكو 87 ، 777-788 (2022). https://doi.org/10.1134/S0006297922080090
- تشاو لي وآخرون 2022. الأدوات والموارد الحاسوبية لتحرير CRISPR / Cas Genome. علم الجينوم والبروتيوميات والمعلوماتية الحيوية. متاح على الإنترنت 24 مارس 2022. DOI: https://doi.org/10.1016/j.gpb.2022.02.006
- van Beljouw، SPB، Sanders، J.، Rodríguez-Molina، A. et al. استهداف RNA لأنظمة CRISPR-Cas. نات ريف ميكروبيول 21 ، 21–34 (2023). https://doi.org/10.1038/s41579-022-00793-y
- تشوني هو وآخرون 2022. Craspase هو بروتياز CRISPR RNA الموجه ، RNA المنشط. علوم. 25 أغسطس 2022. المجلد 377 ، العدد 6612. الصفحات 1278-1285. DOI: https://doi.org/10.1126/science.add5064
- Huo ، G. ، Shepherd ، J. & Pan ، X. Craspase: محرر جيني مزدوج CRISPR / Cas. علم الجينوم الوظيفي والتكامل 23 ، 98 (2023). تاريخ النشر: 23 مارس 2023. DOI: https://doi.org/10.1007/s10142-023-01024-0
***